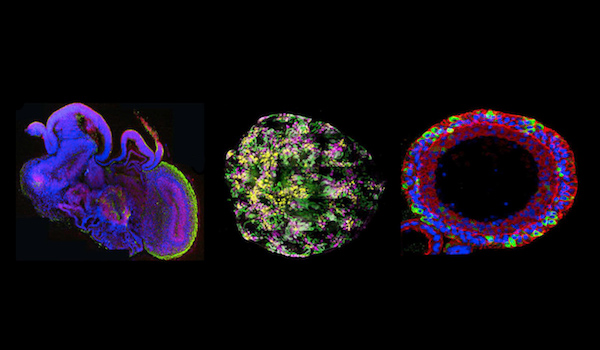
Los organoides son copias diminutas de los órganos de una persona concreta, creados a partir de sus tejidos y células. Su respuesta a un medicamento concreto podría ayudar a predecir si un paciente se beneficiaría de él o no
En mayo, la ministra holandesa de Salud, Edith Schippers, rompió las negociaciones con la empresa de biotecnología Vertex. El problema era el exorbitante precio de su medicamento para tratar la fibrosis quística, Orkambi. Demasiado caro, dijo el ministerio. Y no funciona lo suficientemente bien. Los pacientes tendrán que seguir luchando sin ella.
Pero ahora una coalición de grupos de pacientes, aseguradoras y biólogos holandeses cree que una nueva tecnología podría acabar con la barrera económica. El fármaco podría resultar más rentable si se probara en organoides, unos diminutos grupos de células que se asemejan a los componentes de los órganos humanos (ver TR10: Organoides cerebrales para desentrañar la mente). ¿Cuán pequeño es un organoide? No mucho más grande que el punto final de esta frase.
La semana pasada, unos científicos holandeses contactaron con el Ministerio para presentarle una propuesta para cultivar en sus laboratorios este tipo de miniórganos a partir de células de los 1.500 pacientes de fibrosis quística holandeses. De esa manera, Orkambi y otros fármacos caros podrían probarse en el laboratorio para comprobar si serán eficaces en un paciente determinado. El medicamento sólo se compraría si el organoide de un paciente respondiera bien al tratamiento.
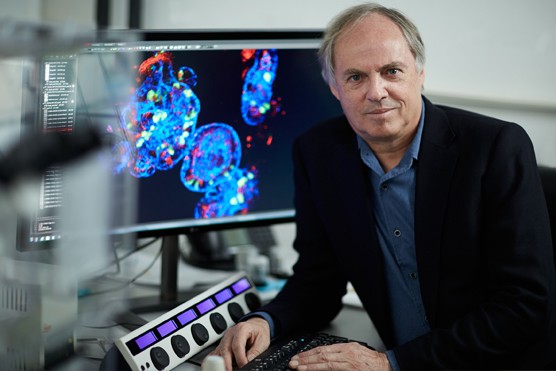
Foto: el científico médico Hans Clevers cree que las pruebas con miniórganos cultivados en el laboratorio podrían ayudar a rentabilizar los medicamentos más caros al identificar a los pacientes con más probabilidades de beneficiarse de ellos
“El organoide actúa como un avatar del paciente”, explica el científico del Instituto Hubrecht que dirige el esfuerzo, Hans Clevers, y añade: “Podemos exponer el miniórgano a estos medicamentos tan caros, ysólo se les recetarían a quienes realmente se beneficiaran de él”.
Si el plan avanza, podría marcar el inicio de una transición en el negocio de los fármacos. Por primera vez, los organoides podrían empezar a usarse para tomar decisiones sobre quién debe tomar los nuevos medicamentos más caros del mundo y quién no. Actualmente estas decisiones se toman a partir de análisis de sangre y síntomas,
Orkambi está diseñado para pacientes con fibrosis quística, causada por un tipo específico de mutación genética. Vertex afirma que los estudios más amplios con el medicamento demuestran que todos los pacientes con esa mutación responden al tratamiento. Por lo tanto, la compañía no avala el plan de los organoides. En su opinión, los grandes estudios con voluntarios siguen representando el “estándar de oro” y “no deben ser reemplazados” por resultados en organoides. El director médico sénior de fibrosis quística de Vertex, Mark Higgins, señala: “La ciencia de los organoides todavía está en fase inicial”
El proyecto holandés nació en el laboratorio de Clevers y en el Centro Médico Universitario de Utrecht (Holanda), donde los científicos aprendieron a tomar una muestra del recto de un paciente y cultivar diminutos trozos de tejido intestinal, con pliegues y vellosidades similares a las que se encuentran en el intestino grueso humano.
El nuevo enfoque analítico implica exponer los organoides a los fármacos de fibrosis quística y comprobar si se hinchan. Esto significa que la causa de la enfermedad se estaría invirtiendo. Pero ahora mismo nadie sabe hasta qué punto un organoide puede predecir la respuesta de un paciente a largo plazo. “Definitivamente, no está claro lo exactos que son”, apunta el un profesor de la Universidad de Boston (EEUU) Finn Hawkins, que trabaja en organoides de pulmón. Pero el experto matiza: “Seré sincero contigo: creo que representan el futuro de la medicina”.
En Holanda, una organización sin ánimo de lucro llamada HUB Foundation for Organoid Technology ya está comercializando la tecnología de Clevers. Sus clientes incluyen a Vertex, que ya está explorando los organoides en sus investigaciones. La empresa tiene dos ensayos clínicos en curso, uno en Holanda y otro en Israel. El objetivo es descubrir la conexión entre las respuestas de los organoides y los pacientes que se beneficiarían del medicamento, y cuánto.
La fibrosis quística podría ser la enfermedad perfecta para probar la tecnología. La dolencia, que produce una acumulación pegajosa en los pulmones y conduce a la muerte prematura, es causada por errores en un gen involucrado en las células que producen la mucosidad, las lágrimas y la saliva. Pero hay más de 2.000 mutaciones diferentes que pueden causar la fibrosis quística, y las farmacéuticas no pueden abordarlas todas.
Los fabricantes de medicamentos han estado compitiendo por desarrollarfármacos de precisión para las mutaciones más comunes. Vertex tiene dos de ellos. Uno, Kalydeco, puede ayudar a uno de cada 25 pacientes. El otro es Orkambi, que ha sido aprobado para la mutación más común de la fibrosis quística, presente en cerca de la mitad de los pacientes.
Ninguno de los dos tratamientos es precisamente barato. Aunque Kalydeco fue aclamado como tratamiento milagroso, un médico calificó su precio inicial de más de 260.000 euros anuales de “desmedido” (ver Historia de dos fármacos (o del negocio farmacéutico)). Orkambi cuesta menos, pero sus beneficios no están tan claros.
En Holanda, donde Kalydeco está en venta, ya se han utilizado organoidespara determinar si debe ser recetado a pacientes con mutaciones ultrarraras que nunca han sido estudiadas en ningún ensayo. El caso de un paciente, un adolescente llamado Fabian, apareció en el popular programa de entrevistas holandés The World Goes On (Aquí hay un video quedescribe su caso.) La mutación genética de Fabian era única, por lo que nunca se había estudiado. Pero los investigadores hicieron un organoide para él y demostraron que Kalydeco funcionaba. Clevers rescuerda: “Nuestro organoide demostró que [Fabian] se beneficiaría”, así que en cuanto el joven empezó a tomar las pastillas, “mejoró en cuestión de horas”, añade.
Vertex cree que identificar a más pacientes que podrían curarse con estos fármacos es la función más adecuada para los organoides. La compañía afirma que hay varios casos en Holanda en los que las aseguradoras están cubriendo el coste de Kalydeco gracias a los resultados de organoides. Pero ahora el debate se centra en Orkambi, y la pregunta es si los organoides acabarían limitando el uso del fármaco en lugar de ampliarlo.
Orkambi está aprobado en Europa, pero su precio de casi 160.000 euros sigue siendo un obstáculo para un país pequeño como Holanda. Según un informe preparado para el Ministerio holandés de Salud por el Zorginstituut Nederland, un instituto que asesora al Estado sobre la relación coste-eficacia, proporcionárselo a todos los pacientes costaría unos 105 millones de euros al año. Pero este gasto no se considera razonable, ya que muchos de los pacientes no obtendrían ningún beneficio.
El instituto sugirió que el fármaco vale un 82% menos de lo que Vertex pide por él. Poco después, las negociaciones entre Vertex y el Ministerio de Salud se rompieron. La representante de los pacientes holandeses con fibrósis quística, Jacquelien Noordhoek, afirma: “No consiguieron llegar a un punto medio, y esto fue una noticia muy, muy mala para nosotros. Y estoy de acuerdo en que el precio era demasiado alto”.
A diferencia de Vertex, los científicos holandeses y las organizaciones de pacientes dicen que, incluso entre los individuos con la mutación correcta,es evidente que el fármaco no funciona igual para todos. Si se cultivara un organiode para cada paciente, sugiere Clevers, el fármaco podría ser dispensado únicamente a aquellos cuyos organoides hayan respondido positivamente. Eso podría hacer que el tratamiento resultara asequible a nivel nacional, a pesar del precio de su etiqueta.
Pero hay un círculo vicioso que podría impedir un estudio de este tipo, ya que el Gobierno holandés primero tendría que asumir el coste del fármaco para que los pacientes pudieran acceder a él. Es por eso que Clevers y Noordhoek acudieron al Ministerio la semana pasada para presionar a favor de su autorización.
Fuente: MIT Technology Review